La Newsletter 15 décembre 2008

– Dans le numéro 170 de Spectra Biologie –
Innovations
COAGULATION >> Gamme de réactifs liquides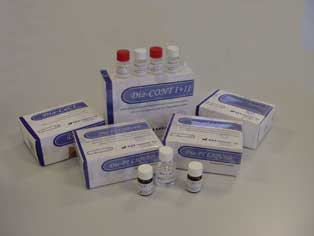
Contrairement à la chimie clinique, la part de marché liée aux réactifs liquides et prêts à l’emploi en coagulation reste encore modeste. La cause étant sans doute la difficulté de production permettant de maintenir des caractéristiques techniques satisfaisantes. Depuis trois ans, Diagon a développé sa propre gamme de réactifs. Le premier réactif de TP liquide produit à partir de cerveau de lapin a prouvé ses performances sur des coagulomètres utilisant des principes de mesure différents (viscosité, néphélométrie, turbidimétrie). L’intervalle de l’ISI (International Sensibility Index) de ce réactif se situe entre 1,1 et 1,25 en fonction du principe de mesure. La traçabilité est assurée avec le réactif de référence international WHO RBP. La stabilité à 4–8 °C du réactif liquide Diagon avant ouverture est d’un an avant ouverture (une semaine après ouverture). Il est conditionné en doses de 2mL. Les coefficients de variation obtenus à partir de coagulomètres semi-automatiques sont inférieurs à 2 %. Le second réactif de la société est l’APTT (ou TCA) qui utilise l’acide ellagique comme activateur. Il a été spécialement mis au point pour des analyseurs utilisant un principe de mesure optique. Là aussi, les résultats obtenus ont un CV de moins de 2 % avec une stabilité de deux semaines à 4–8 °C après ouverture. • Site du fabricant
IMMUNOCHIMIE >> Offre consolidée immunochimie-biochimie
L’évolution des structures dans le domaine de l’analyse médicale est en cours. Thermo Fisher Scientific adapte donc son offre. Afin de répondre aux besoins des laboratoires, un accord de partenariat a été conclu avec la société Tosoh Bioscience. L’objectif : proposer une solution commune s’appuyant sur les savoir-faire respectifs des deux entreprises. Le système Korus est ainsi décliné en trois modèles adaptés aux laboratoires souhaitant une consolidation biochimie et immunochimie, ainsi qu’une première approche de l’automatisation. En plus de ses fonctions analytiques, le Korus permet en effet le tri des tubes et leur débouchage, libérant les utilisateurs et évitant l’exposition au risque biologique. Les trois modèles sont : le Korus (180 tests par heure en immunologie et 600 tests par heure en biochimie), le Korus Advance (cadences identiques plus module déboucheur), et le Korus Plus (180 tests par heure en immunologie, 1 200 tests par heure en biochimie plus module déboucheur). Toute la gamme a officiellement été lancée lors des JIB 2008 au mois de novembre dernier.• Site du fabricant
INFORMATIQUE DE LABORATOIRE >> Nouvelle version de solution « middleware »
Depuis sa 1re version en 2001, le logiciel MPL de Roche Diagnostics n’a pas cessé d’évoluer. La 3e génération, MPL EVO, sera disponible au début de 2009. Il s’agit d’une vraie solution « middleware » de gestion de production des laboratoires grâce à de nouvelles capacités de gestion multi-sites. Il est connectable à plusieurs systèmes de gestion de laboratoire différents, autour d’une base de donnée unique et centralisée, avec une gestion des utilisateurs adaptée à la nouvelle dimension des plateaux techniques. Un autre atout de MPL EVO est le management de la production. Il informe en temps réel de toute anomalie des délais d’arrivée des tubes et des délais de production (temps pré-analytique, temps de validation, temps de rendu, TAT etc.). Grâce à des informations en temps réel et à des « widgets » personnalisables, des informations visuelles, il s’affiche sur n’importe quel écran d’ordinateur. MPL EVO contribue à un meilleur contrôle de l’organisation des laboratores, par un outil de suivi de tubes intra- et inter-sites, par des outils de supervision de la connectique (SIL automates, poste) et par une gestion avancée des droits utilisateurs. La solution de Roche Diagnostics aide également à répondre aux exigences de l’accréditation par sa gestion automatique des lots de réactifs, de calibrants, et de contrôles en garantissant la traçabilité, de l’arrivée dans le laboratoire jusqu’à leur utilisation. Afin d’apporter une analyse toujours plus pertinente, de nouvelles fonctions s’ajoutent afin d’éviter des analyses inutiles et fausses, et pour mettre en regard les opérations de maintenance et les changements de lots.• Site du fabricant
INFORMATIQUE DE LABORATOIRE >> Module d’aide à l’interprétation thérapeutique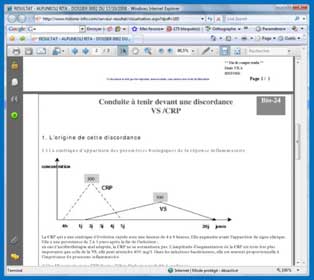
Le rôle de conseil du biologiste auprès du prescripteur devient de plus en plus important, cela étant confirmé par le rapport Ballereau. Histone propose un nouveau module pour son système informatique de gestion LAM 400a, le module e-EXPERT qui répond à ces prérogatives. Il possède en effet des fonctions permettant au biologiste de posséder un outil d’expertise en matière d’interprétation des résultats patients. Grâce au paramétrage de différentes règles, le système permet d’automatiser la logique du raisonnement lors de la validation du résultat : analyse de la cohérence médicale des paramètres d’un dossier (corrélation inter-analyses), variation par rapport au résultat précédent, intégration d’une pathologie du patient. De plus, à l’aide d’une base de données documentaires fournie sous forme de fiches .pdf le biologiste peut inclure manuellement ou automatiquement des informations à destination du prescripteur dans les compte-rendus transmis. Cette base de données peut évidemment être modifiée et enrichie par le biologiste. Le module e-EXPERT et le logiciel LAM 400 constituent donc un système efficace et aux fonctionnalités étendues.• Site du fabricant
INFORMATIQUE DE LABORATOIRE >> Logiciel universel de connexion d’analyseurs 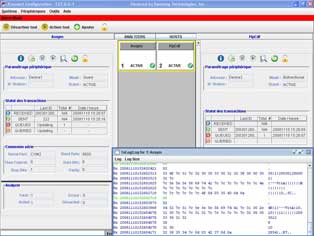
JConnect de la société Intertecnica établit une connexion simple entre l’analyseur et le SGL (Système de Gestion du Laboratoire), avec un excellent rapport qualité/prix. JConnect est le logiciel d’entrée de gamme de la série JResultNet et il hérite de ce fait d’une importante librairie de drivers de connexion. Il supporte, côté SGL, une large gamme de protocoles (ASTM, HL7, XML, CSV, CDF, HPRIM, connexion directe à la BD). L’interface utilisateur (GUI) permet de gérer aisément une connexion SGL-analyseur au moyen de modules graphiques. Il est possible à tout moment d’évoluer vers les versions supérieures de JResultNet. JConnect sera disponible au début de l’année 2009.• Site du fabricant
INFORMATIQUE DE LABORATOIRE >> Serveur de données médicalisées Inter- et Intranet
Entièrement multimédia, qu’il soit sur site ou à distance, le serveur LEO de PACT Le Cabinet Richard, intègre, traite, diffuse et met à disposition les données des professionnels de santé, quels que soient leur systèmes informatique de gestion et leur discipline, sous forme de texte, d’images et de sons. Les transactions sont sécurisées par un système de cryptage garantissant la confidentialité des données en circulation sur le Net. Un système de traçabilité des actions sur le serveur permet de savoir, à tout moment, qui a fait quoi et quand cela a été fait. L’accès à LEO est contrôlé par lecture des cartes CPS. Les normes d’échanges HL7 France et HPRIM sont utilisées comme dans 98 % des progiciels installés chez les professionnels de santé. Le serveur supporte les principaux navigateurs Internet (Internet Explorer, Mozilla, Safari). Il met à la disposition des requêtes de calculs statistiques pour le suivi des patients et des données médico-administratives. LEO permet également l’impression à distance des résultats et l’envoi automatique de courriels cryptés.• Site du fabricant
INFORMATIQUE DE LABORATOIRE >> Module informatique dédié à l’archivage
Progimed complète son offre en créant pour l’ensemble de sa gamme un module dédié à l’archivage. Très simple d’utilisation, cet outil permet au laboratoire de gérer de manière autonome et personnalisée ses archives. Qu’il s’agisse de journaux (légaux, caisses…), de résultats nominatifs (avec images scannées), de procédures qualité ou de factures liées à la gestion des stocks, le directeur du laboratoire ou le qualiticien pourront retrouver les archives et les conserver sur la période souhaitée. Elles peuvent être stockées sur un ordinateur dédié ou sur un support optique (DVD ou CD). Grâce à un simple navigateur Internet la consultation s’effectue de manière ergonomique et indépendamment du système de gestion de laboratoire. Le module d’archivage facilite le respect d’obligation de conservation des données et constitue une réponse aux exigences de sécurisation des données écrites par les différents référentiels de qualité.• Site du fabricant
INFORMATIQUE DE LABORATOIRE >> Suite logicielle complète sous Linux
Déjà présent sur le marché des groupements de laboratoires avec une solution innovante de partage d’automates (middleware MCA) , Clarisys Informatique dispose désormais d’une suite complète de gestion de laboratoire grâce à Clarilab. Il s’agit d’un SGL de toute dernière génération, conçu pour une gestion optimale des groupements de laboratoires, quelles que soient leurs tailles et leur organisation. Intégrant un FSE 1.40, une traçabilité complète, un module de gestion/transfert comptable, un serveur de résultat Intranet, Clarilab se place parmi les SGL modernes. En recourant aux technologies GNU/Linux, Clarisys informatique garantit à ses utilisateurs de disposer en toute circonstance d’une solution sécurisée, stable et perenne. Grâce à sa conception récente avec des technologies innovantes, Clarilab répond à l’ensemble des recommandations de l’ISO 15189 et constitue un atout pour les laboratoires dans leur démarche d’accréditation.• Site du fabricant
ONCOLOGIE >> Kit ELISA CgA
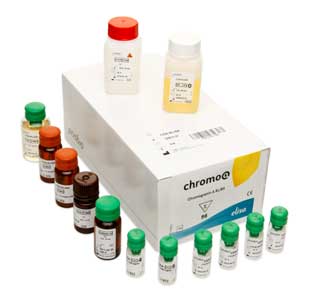
Cisbio Bioassays, société qui développe et commercialise des tests diagnostics pour la quantification de marqueurs tumoraux a lancé un nouveau kit ELISA chromogranine A (CgA), nommé Chromoa™. Ce kit utilise des anticorps monoclonaux mettant en évidence une augmentation du taux de protéines sériques lors du développement d’une tumeur neuroendocrine. Ce type de tumeur touchent le plus souvent la glande surrénale, le pancréas et le tractus gastro-intestinal. La chromogranine A est un analyte adopté pour la détection et le suivi de ces tumeurs et de certains cancers de la prostate, qui peuvent évoluer vers une différenciation neuroendocrine agressive. Le kit ELISA est basé sur les mêmes anticorps que le CGA-RIACT, déjà commercialisé depuis une dizaine d’années. Cisbio fait partie du groupe belge IBA depuis le mois de mai dernier.
• Site du fabricant
ONCOLOGIE >> Test immunochromatographique de dépistage précoce du cancer de la vessie
Avec une incidence de 350 000 nouveaux cas par an dans le monde (dont 12 500 en France), la cancer de la vessie occupe la deuxième place des cancers urologiques après celui de la prostate. Son diagnostic précoce est essentiel afin d’améliorer le pronostic vital : 70 % des tumeurs correspondent à des formes superficielles, et 30 % à des formes invasives avec atteintes de la musculeuse. Inverness Medical France complète sa gamme en oncologie avec un test rapide permettant la détection qualitative de la NMP22® (Nuclear Matrix Protein 22), un marqueur tumoral utilisé dans le dépistage et la surveillance de patients atteints d’un cancer de la vessie. La sensibilité de ce test peut atteindre 85 % et sa spécificité 95 %, des résultats qui améliorent ceux des cytoscopies et de la cytologie urinaire. Le test NMP22 BladderChek est un test immunochromatographique sur bandelette qui est utilisé avec des échantillons d’urine. Il se présente sous le forme de cassettes et ne nécessite que quatre gouttes d’urine pour un résultat en 30 minutes. Rapide, fiable, non invasif et de faible coût, ce test constitue donc une aide pour le diagnostic du cancer chez les patients à risque. Le test NMP22 est également disponible sous la forme de microplaques ELISA pour un dosage quantitatif de la protéine par méthode immuno-enzymatique.• Site du fabricant
SERVICE >> Programme de contrôle qualité externe
 Le vaste programme Riqas de Randox (Randox International Quality Assessment Scheme) permet aux biologistes d’analyser leurs performances analytiques de manière simple et rapide. Avec plus de 8 100 participants à travers le monde, et grâce à une plage de programme très large, Riqas apporte la confiance nécessaire aux résultats des laboratoires. Tous les programmes sont accrédités ISO 13485 et UKAS. Plus qu’un simple programme de contrôle qualité externe, Riqas est une solution qui aide à l’obtention de l’accréditation. Dès janvier 2009, de nouveaux programmes seront disponibles : Coagulation, Cardiac liquide, Gaz du sang, Hormones de grossesse, Urines toxicologie et Urines bandelettes. En tout, seize programmes destinés à améliorer les performances des biologistes, pour assurer un suivi patient optimum et faciliter les démarches d’accréditation.
Le vaste programme Riqas de Randox (Randox International Quality Assessment Scheme) permet aux biologistes d’analyser leurs performances analytiques de manière simple et rapide. Avec plus de 8 100 participants à travers le monde, et grâce à une plage de programme très large, Riqas apporte la confiance nécessaire aux résultats des laboratoires. Tous les programmes sont accrédités ISO 13485 et UKAS. Plus qu’un simple programme de contrôle qualité externe, Riqas est une solution qui aide à l’obtention de l’accréditation. Dès janvier 2009, de nouveaux programmes seront disponibles : Coagulation, Cardiac liquide, Gaz du sang, Hormones de grossesse, Urines toxicologie et Urines bandelettes. En tout, seize programmes destinés à améliorer les performances des biologistes, pour assurer un suivi patient optimum et faciliter les démarches d’accréditation.
• Site du fabricant
PARASITOLOGIE >> Test de diagnostic rapide de la malaria
Le paludisme est aujourd’hui la parasitose tropicale la plus répandue dans le Monde. Une maladie qui peut s’avérer mortelle si une thérapie adaptée n’est pas mise en place rapidement. Son diagnostic conventionnel repose sur l’observation au microscope du sang total et requiert un personnel qualifié. Un diagnostic demandé en urgence peut s’avérer délicat lorsque seule l’interprétation de la goutte épaisse est disponible. L’immunochromatographie propose une alternative permettant au biologiste de conforter et d’orienter un résultat de façon fiable et rapide. Le test Binax Now® Malaria d’Inverness Medical constitue donc un outil de choix. Facile d’utilisation, il permet d’effectuer la différenciation entre le Plasmodium falciparum et trois autres espèces en 15 minutes. La sensibilité revendiquée est de 100 % et la spécificité de 96 %. À l’heure actuelle, le test rapide Binax Now Malaria est le seul à avoir reçu l’accréditation FDA.• Site du fabricant
VIROLOGIE >> Analyseur pour le comptage des lymphocytes T CD4
Inverness Medical Solutions a présenté son analyseur pima™ à la 15e Conférence sur le Sida et les infections sexuellement transmissibles en Afrique (CISMA). Il s’agit d’un système unique pour le comptage des lymphocytes T CD4, car le comptage de ces cellules est une étape critique pour l’évaluation du système immunitaire des personnes séropositives. Pour les cliniciens, ce comptage est un moyen de démarrer rapidement un traitement antiretroviral approprié (ARV). Le comptage régulier des lymphocytes T CD4 pendant le traitement permet de juger de la progression de la maladie et des résultats des antirétroviraux. Simple d’utilisation, fonctionnant sur batteries, la plateforme pima est une première solution délocalisée. Elle utilise le même principe d’analyse statique des images que les systèmes classiques, mais dans un format compact. La technologie utilisée dans la cassette permet un comptage des lymphocytes T CD4 en moins de 20 minutes sur un échantillon de sang collecté au doigt. Les essais cliniques sont en cours et l’instrument devrait être disponible à la mi-2009.• Site du fabricant
VIE DES SOCIETES >> bioMérieux : filiale dubaïote et expansion américaine
Le groupe français bioMérieux a annoncé l’ouverture de sa 39e filiale internationale : implantée à Dubaï, dans les Emirats Arabes Unis, elle servira de plateforme pour les opérations au Moyen-Orient où la société était déjà présente depuis 25 ans. Sur place, elle continuera de travailler avec son distributeur exclusif Al Hayat Pharmaceuticals. Dubaï est appelé à devenir une place importante dans la région avec l’édification de la « HealthCare City », une zone franche qui devrait abriter 20 000 professionnels de la santé, et l’implantation d’institutions internationales telles que la Harvard Medical School et la Mayo Clinic. bioMérieux apportera en particulier son expertise dans le domaine de la lutte contre les infections nosocomiales aux universités et hôpitaux locaux. D’autre part, le groupe hexagonal a été récompensé par le cabinet Frost & Sullivan pour son « leadership » dans le domaine de la microbiologie pharmaceutique sur le marché nord-américain ». Ayant récolté 10,13 points sur 12, la société s’est classée au premier rang dans trois catégories : croissance et positionnement sur le marché, atouts, capacités d’innovation et stratégie de croissance. D’ailleurs, dans ce dernier dernier domaine, vient encore une fois de démontrer son dynamisme en réalisatnt l’acquisition de l’entreprise américaine PML. Cette dernière basée à Wilsonville dans l’Orégon est spécialisée dans les milieux de culture et les produits de contrôle microbiologique destinés aux applications cliniques et industrielles.• Site de la société
VIE DES SOCIETES >> Septin 9 un biomarqueur stratégique
La société de biotechnologie allemande Epigenomics et Abbott Molecular ont annoncé l’extension de leur partenariat stratégique non-exclusif concernant le développement et la commercialisation d’un test de diagnostic moléculaire pour la détection précoce du cancer colorectal. Cette signature permet à Abbott Molecular d’obtenir des licences additionelles pour l’utilisation de la technologie propriétaire d’Epigenomics fondée notamment sur l’analyse des profils de méthylation de l’ADN d’un biomarqueur, le gène Septin 9. De plus la société pourra bénéficier d’un accès aux échantillons de sang collectés dans le cadre de l’étude multicentrique PRESEPT mise sur pied par Epigenomics afin d’évaluer l’intérêt du marqueur Septin 9 et sa capacité à satisfaire les recommandations américaines concernant le dépistage du cancer colorectal. Les deux partenaires ont travaillé au développement de ce test pour une utilisation sur le système de diagnostic moléculaire m2000 d’Abbott. Ils misent sur l’obtention du marquage CE et le lancement de ce test en Europe pour la fin de l’année 2009.• Site de la société
VIE DES SOCIETES >> Dako-Genentech, un nouvel accord théranostic
Dix ans après avoir posé la première pierre de la collaboration qui devrait mené à la mise au point de l’herceptin, le premier médicament issu de la pharmacogénomique, les sociétés Genentech et Dako ont annoncé la signature d’un nouveau partenariat. Comme il y a dix ans les deux partenaires comptent mettre à profit le savoir de Dako dans le domaine du diagostic du cancer afin d’élaborer un test qui pourra potentiellement servir de tes compagnon à une molécule anticancéreuse aujourd’hui en cours de développement dans les laboratoires de Genentech. Ce nouvel accord révélateur de l’intérêt actuel des industriel pour le théranostic, avait été précédé d’une autre entente du même type entre la société danoise et le groupe pharmaceutique Bristol-Myers Squibb.• Site de la société
PROFESSION >> Évolution des recommandations sur les tests VIH
La Haute Autorité de Santé (HAS) vient de publier le premier volet de ses recommandations en santé publique sur le dépistage du VIH en France. Il comporte des recommandations sur les modalités de réalisation des tests de dépistage chez l’adulte et l’enfant de plus de 18 mois, et des orientations sur la place et sur les conditions d’utilisation des tests de dépistage rapide. Aujourd’hui, le diagnostic biologique de l’infection est réalisé en deux temps : une analyse de dépistage permet de détecter les anticorps anti-VIH. Toute analyse positive doit être complétée par une confirmation réalisée sur le prélèvement sanguin initial. L’analyse de confirmation permet, d’une part, de vérifier que les anticorps sont bien liés à une infection par le VIH, et d’autre part, elle d’identifier le type de virus présent (VIH 1 ou 2). Désormais, la HAS recommande de n’utiliser qu’une seule technique contre deux auparavant : le test combiné Elisa a été reconnu plus performant au début de l’infection. De plus, une personne sera considérée comme « non infectée » si ce test est négatif au bout d’une période de six semaines après l’exposition supposée au virus et non plus douze semaines. En revanche, si la personne prend un traitement préventif suite à une exposition supposée, le test de dépistage devra être réalisé trois mois après l’arrêt de ce traitement, comme c’est déjà le cas actuellement. Concernant les tests de dépistage rapide, leur utilisation est recommandée dans certains cas d’urgence médicale tels que les accidents professionnels d’exposition au sang ou les accidents d’exposition sexuelle, après recueil du consentement éclairé de la personne. Aisément réalisables, il permettent d’obtenir un résultat en moins de 30 minutes à partir d’un échantillon de sang total, de salive, de sérum ou de plasma. Quoi qu’il en soit leur utilisation implique le respect de conditions précises de mise en œuvre afin de garantir la qualité du résultat obtenu et tout résultat positif doit faire l’objet d’un test de confirmation.
En dehors ces situations d’urgence, la HAS reconnaît également l’intérêt de ces tests rapides pour faciliter l’accès au dépistage à certaines populations dépourvues d’accès aux dispositifs traditionnels de dépistage.
Un second volet de recommandations sera publié pendant le premier semestre de l’année 2009 pour évaluer la pertinence d’une évolution des stratégies et du dispositif de dépistage du VIH, notamment la mise en place d’un dépistage de routine (étendu à toute la population, en dehors de tout comportement à risque) dans certaines régions spécifiques (Guyane).• Site de l’agence
PROFESSION >> Réseau Next Lab, façonné par les biologistes
Evolutions réglementaires et économiques, pression concurrentielle accrue impliquant aujourd’hui des groupes internationaux très structurés… Le secteur de la biologie française est entré dans une phase de restructuration profonde. Dans ce contexte éclosent des projets issus de la profession et destinés à lui permettre de défendre ses valeurs au travers de nouvelles formes d’organisation. La structure Next Lab, créée en juillet 2008, constitue l’une de ces initiatives et résulte d’une réflexion menée par une vingtaine de biologistes membres du Réseau de Biologie Moléculaire Libérale (RBML). Le projet défini par ces praticiens s’appuie sur quatre idées maîtresses : une entreprise façonnée par les biologistes proche du patient et dégageant une image scientifique et médicale forte ; la mise en place d’une structure opérationnelle fondée sur le regroupement d’entités régionales exerçant de façon autonome ; une structure juridique conçue pour que les biologistes restent les décideurs ; un montage financier s’appuyant sur un rachat par effet de levier (LBO, Leverage Buy Out) construit sur sept ans.
La dimension nationale du projet permet à ses membres de rompre leur isolement et de disposer des moyens d’évoluer dans un environnement concurrentiel renforcé en profitant de la masse critique offerte par le réseau (capacité d’économie d’échelle, notoriété accrue, synergies d’idées,…). Conçu comme une holding constituée sous la forme d’une SAS, Next Lab compte aujourd’hui un actionnariat composé de 11 biologistes ouvert aux autres professionnels souhaitant les rejoindre. La société Next Lab détiendra à terme 90 % des parts de chacune des structures régionales constituant son réseau. Ses statuts assurent aux biologistes un minimum de 75 % de parts réservés et intègrent des principes de gouvernance pérennisant leur pouvoir de décision. La présence, plafonnée à 25 %, d’un partenaire financier permet notamment le départ dans des conditions favorables des associés candidats à la retraite et l’apport de ressources financières nécessaires au développement du réseau. Pour mener à bien ce projet ses créateurs misent sur un calendrier serré avec une année 2009 consacrée à la préparation et à la construction des structures régionales, l’intégration de celles-ci en 2010 puis, une fois cette deuxième étape terminée, l’entrée au capital du partenaire financier.
PROFESSION >> Naissance de la Fédération Euro-Méditerranéenne des LABM
Fédérer les biologistes euro-méditerranéens… Cette idée essentielle pour donner à la profession un poids politique renforcé est désormais concrétisée. La Fédération Euro-Méditerranéenne de Biologie Médicale (FEMLAB), a été officiellement lancée avec la signature de ses statuts le 7 novembre à Paris lors des denières JIB. Ses objectifs ? Promouvoir un exercice de la biologie clinique commun à tous les pays du pourtour méditerranéen. La présidence a été confiée à Jean Benoît (président du Syndicat des Biologistes français), El Houssine Bennani (président de la Chambre syndicale des biologistes marocains) assure la vice-présidence et Bahri Cherif (président du Syndicat des biologistes tunisiens) le secrétariat général. Au mois de juin déjà, les 22es journées de biologie clinique de Tunisie (Hammamet) avaient permis la rencontre des syndicats d’Italie (Federlab), d’Algérie, du Maroc, de France, du Liban et de Tunisie. Les instances comprennent un bureau executif de six membres (trois praticiens des rives nord de la Méditerranée et trois des rives sud), un conseil consultatif (membres de droit, membres associés et membres honoraires) et une assemblée consultative réunissant l’ensemble des cotisants. Ce projet, qui s’inscrit parfaitement dans la perspective de l’Union pour la Méditerranée, devrait contribuer à la création d’une identité régionale forte garantissant l’équilibre et le partage Nord-Sud, ainsi que la promotion d’un exercice libéral mettant l’exergue sur la relation praticien-patient.
Composition du bureau exécutif : Jean BENOIT (France), président ; El Houssine BENNANI (Maroc), vice-président ; Bahri CHERIF (Tunisie), secrétaire général ; Vincenzo D’ANNA (Italie), secrétaire général adjoint ; Hachmi OULD ROUIS (Algérie), trésorier ; Jorge Nunes DE OLIVEIRA (Portugal), trésorier adjoint.
Autres Membres fondateurs : Smail BELAZZOUG (Algérie), Camilo Fernandez ESPINA (Espagne), Jean BEGUE (France), Corrado MARINO (Italie), Adel MASTORI et Marc-Antoine ZABLITH (Liban), Mohamed BENAZZOUZ et Youssef IDRISSI KAITOUNI (Maroc), Naoufel NABLI (Tunisie), Jean-Pierre MOLGATINI (Confédération des Biologistes Européens).• Site de l’association
SCIENCES >> Un nouveau mécanisme de résistance à la dengue
Dans la majorité des cas, la dengue est une infection virale bénigne, voir asymptomatique. Cependant, il est de plus en plus fréquent d’observer le développement d’un syndrome hémorragique mortel, surtout chez les enfants pendant les périodes épidémiques. Des chercheurs du CNRS, de l’Institut Pasteur et de l’université de Berkeley (Californie) ont publié des travaux mettant en évidence un mécanisme de résistance au virus de la dengue. Les cellules dendritiques de la peau seraient les premières cibles de ce virus au site d’inoculation par le moustique vecteur. L’interaction entre la glycoprotéine de l’enveloppe virale et une molécule de surface (CD209/DC-SIGN) des cellules dendritiques constituerait un événement crucial pour l’infection. Les macrophages du derme humain exprimant cette protéine seraient capables de capturer le virus de la dengue sans qu’il soit en mesure de s’y multiplier. Cette inhibition inattendue consituerait un important système de défense innée contre le virus de la dengue chez l’Homme. Chaque année, cette maladie affecte plus de 100 millions d’individus dans les régions infestées par le moustique Ædes ægypti).
SCIENCES >> Un gène altéré responsable du neuroblastome
L’altération du gène Alk serait étroitement associée au développement de la tumeur solide extra-cérébrale la plus fréquente chez l’enfant : le neuroblastome. C’est ce que révèle une étude menée par une équipe Inserm de l’Institut Curie (Unité 830 « Génétique et biologie des cancers ») : le gène Alk, qui code pour un récepteur à activité tyrosine kinase présent à la surface cellulaire, serait même un gène de prédisposition familiale. Près de 600 prélèvements de neuroblastomes ont ainsi été analysés. Tous présentaient une altération du gène Alk, soit par augmentation du nombre de copies, soit par mutations activatrices. Son inhibition dans des cellules de neuroblastome entraînerait à l’inverse une forte baisse de la prolifération cellulaire. La découverte de la transmission de ces mutations à la descendance, confirmée par une équipe américaine devrait permettre de pouvoir identifier dans les familles à risque les enfants porteurs, d’effectuer une surveillance adaptée et d’obtenir un diagnostic plus précoce. Le gène Alk serait également impliqué dans certains lymphomes et un type de cancer du poumon, et des molécules contrecarrant son effet seraient déjà identifiées. Un espoir pour les jeunes patients car la progression rapide du neuroblastome n’est pas enrayée par les chimiothérapies actuellement disponibles.
Manifestations
>> 1er Congrès algérien de Biologie clinique – 2es journées internationales francophones de Médecine de laboratoire
Alger (Algérie) – 1er–3 mai 2009 • Site Web des organisateurs
>> 26e CORATA IBS
Marne-la-Vallée – 26–28 mai 2009 • Site Web des organisateurs
>> 29es Journées normande de Biologie clinique
Palerme (Sicile) – 6–12 juin 2009 • Contact E-Mail
>> Journées de Biologie d’Aquitaine
Biarritz – 11–12 juin 2009 • Contact E-Mail
>> 12e MedLab arabe – 3e Congrès de Biologie clinique du Liban
Beyrouth (Liban) – 6–12 juin 2009 • Site Web des organisateurs
| _________________________________________________ |
| La Newsletter Spectra Biologie est une publication des éditions PCI 176, rue du Temple – 75003 Paris www.editions-pci.com– pci@editions-pci.fr Pour recevoir gratuitement cette Newsletter inscrivez-vous : Inscription |
