 |
10 mars 2010 | |
 |
||
 |
– Dans le numéro 178 de Spectra Biologie –
 |
Innovations |
BACTERIOLOGIE Test rapide pour la détection des Shiga Toxines 1 et 2 d’E. coli
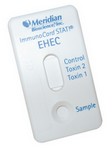
La société Meridian Bioscience fabrique et distribue un nouveau test unitaire à flux latéral pour la détection simple et rapide des Shiga Toxines 1 et 2 d’E. coli sur bouillon de culture à partir de selle. Les souches E. coli entérohémorragiques (EHEC) peuvent être responsables d’infections digestives sévères pouvant évoluer d’une simple diarrhée vers un Syndrome Hémolytique et Urémique (SHU). Cette affection, caractérisée par une insuffisance rénale majeure, touche particulièrement les jeunes enfants et les personnes âgées. Le traitement empirique de cette infection par les antibiotiques augmente le risque de survenue de SHU. L’ImmunoCard STAT!® EHEC commercialisé avec un bouillon Mac Conkey est le premier test unitaire permettant de détecter en 20 minutes les Shiga Toxines de toutes les souches EHEC tout en assurant la différenciation entre les Shiga Toxine 1 et 2. Les performances du test sur bouillon de culture sont caractérisées par une sensibilité de 92,1 % et une spécificité de 100 %.
INFORMATIQUE Application iPhone pour le suivi des analyses

Roche Diagnostics a lancé iMPLevo, une nouvelle application iPhone destinée aux laboratoires de biologie médicale. iMPLevo permet de suivre les données des analyses en cours tube par tube et en temps réel. Cette application est destinée aux laboratoires équipés de la version Ultimate de la solution MPLevo. Elle indique les nombres de tubes arrivés, de tubes en cours d’analyse, de tubes à valider et de tubes traités par laboratoire, par secteur, par discipline ou par automate. Différents calculs peuvent également être réalisés : ceux des délais pré-analytiques (moyenne du jour et de la dernière heure), celui du temps de rendu des résultats (moyenne du jour et de la dernière heure), le temps de validation biotechnique (moyenne du jour et de la dernière heure) et le temps global de rendu de résultats ou TAT, (moyenne du jour et de la dernière heure). La disponibilité de ces paramètres en tous lieux, à tout moment, autorise un suivi très étroit de l’activité du laboratoire et permet au biologiste de repérer et de corriger tout dysfonctionnement nuisible à la délivrance des résultats attendus, en alertant les équipes sur site. iMPLevo permet de connaître la qualité de service rendu aux patients et aux prescripteurs. Pour de nombreuses pathologies, la mise à disposition rapide des résultats permet au médecin de répondre aux urgences, prendre les décisions qui s’imposent, ajuster rapidement un traitement…
INFORMATIQUE Assistant clinique mobile
Panasonic a lancé une nouvelle version de son assistant clinique mobile (MCA pour Mobile Clinical Assistant), le Panasonic Toughbook CF-H1 mk2, doté en option d’un lecteur de cartes à puce intégré. Les médecins et le personnel soignant peuvent donc désormais insérer les cartes à puce pour se connecter au CF-H1 mk2 et enregistrer des informations concernant un patient et par la suite accéder à celles-ci sur place ou lors d’un déplacement. Le CF-H1 mk2 est basé sur la plate-forme de référence de l’assistant clinique mobile Intel® et exploite le processeur Intel® Atom™. Léger et désinfectable, le CF-H1 est un ordinateur portable qui résiste aux chocs comme aux chutes et répond aux normes de contrôle infectieux. Il satisfait aux plus hautes exigences du milieu hospitalier en matière de mobilité et de travail en réseau. Ainsi, il permet aux médecins et au personnel soignant de bénéficier d’un accès instantané aux dossiers médicaux sur le lieu de délivrance des soins, d’obtenir des informations mises à jour sur l’état de santé et les traitements du patient et d’améliorer l’efficacité des protocoles cliniques. En proposant désormais une solution de lecture à contact des cartes à puce ou une lecture sans contact, le CF-H1 mk2 se révèle idéal pour les établissements souhaitant migrer d’une connexion à contact vers une connexion à distance.
METROLOGIE Télérelève de paramètres physiques

Oceasoft, société française spécialisée dans le domaine de la télérelève de paramètres physiques, vient de mettre au point la version 2 du Cobalt. Très simples à installer et à utiliser, les modules Cobalt 2 permettent désormais le contrôle de la concentration de CO2 et de la température avec un seul et même capteur. Le cobalt 2 est également le premier système radiofréquence fonctionnant sur pile longue durée réalisant des mesures de pression différentielle. Il intéresse tout particulièrement le milieu de la santé, laboratoires de biologie médicale, laboratoires pharmaceutiques, les salles blanches et les laboratoires de fécondation in vitro. Les autres évolutions de ce système concernent notamment : l’optimisation des temps de réveil des modules radio (économie d’énergie et durée de vie des piles plus importante, jusqu’à deux ans), la maintenance facilitée grâce à de nouveaux systèmes de fixation (trappe pour les piles, support de module, etc.)… Cet appareil dispose d’un certificat d’étalonnage accrédité Cofrac. Grâce à la transmission radiofréquence numérique, les données enregistrées par le Cobalt 2 sont envoyées vers un PC d’acquisition intégrant un logiciel de contrôle, d’alerte et d’archivage : le thermo-server. Ce logiciel fonctionne en mode client-serveur et il est donc possible de visualiser les mesures et les alertes en toute simplicité et depuis n’importe quel poste du réseau.
EQUIPEMENT DE LABORATOIRE Système de centrifugation innovants
AWEL, fabricant situé à l’Ouest de la France (Nantes et Château-Gontier), lance sur le marché français et à l’international, une gamme de centrifugeurs de laboratoire innovants respectueux de l’environnement. Fort d’une expérience et d’une expertise de plus de 25 ans en conception et industrialisation de centrifugeurs de laboratoire, AWEL propose une dizaine de centrifugeurs (classiques & multifonctions) intégrant des dispositifs innovants répondants aux attentes des utilisateurs en matière d’ergonomie et de productivité. Les centrifugeurs AWEL ont été étudiés et créés pour une installation et une validation sur site en réponse aux exigences normatives et d’accréditations (cGMP, BPL, GBEA…). Le programme de développement de la gamme s’est traduit par le dépôt de 4 brevets en 2009.
VIROLOGIE Gastro-entérites, un test de détection simultanée des rotavirus et adénovirus
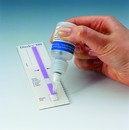
Fumouze Diagnostics propose un test immunochromatographique, Diarlex MB, pour la détection simultanée des rotavirus et des adénovirus dans les selles. L’utilisation conjointe du test Diarlex MB avec le coffret Entérofiltres facilite le prélèvement, le transport et la filtration de l’échantillon de selles. Ce système permet le recueil des selles, même très liquides, à l’aide d’une cuillère puis la filtration dans une solution tampon. L’échantillon dilué se conserve ensuite 10 jours de +2 à +8°C. Le support de bandelette fourni avec le coffret Diarlex MB assure l’hygiène et la traçabilité du test. En 10 minutes, l’apparition d’une ligne rouge signe la présence de rotavirus et une ligne bleue la présence d’adénovirus, une ligne contrôle permet la vérification du bon fonctionnement du test. Deux contrôles positifs internes, adénovirus et rotavirus, sont disponibles et garantissent l’objectivité de la lecture.
 |
 |
Actualités |
VIE DES SOCIETES Abbott se lance dans les LIMS
Acteur d’importance dans les domaines du diagnostic et de la thérapeutique, Abbot étend désormais son portefeuille au secteur de l’informatique de laboratoire. Le groupe américain a en effet annoncé à la mi-décembre 2009 le rachat de la société israélienne Starlims, un des principaux éditeurs de logiciels de gestion d’informations de laboratoire ou LIMS (Laboratory Information Management System) au niveau mondial, pour un montant de 123 millions de dollars, soit 90 millions d’euros. La solution phare de la société israélienne, le progiciel Starlims, intéresse de nombreux types de laboratoires bien au-delà du seul secteur de la santé (environnement, chimie et pétrochimie, agro-industries). Abbott mise toutefois sur cette acquisition pour offrir aux professionnels de santé, des applications informatiques permettant de stocker, d’extraire et d’analyser des données cliniques ou encore des données administratives et/ou de gestion. Selon les dirigeants d’Abbott, les fonctionnalités de Starlims permettront notamment aux laboratoires cliniques de disposer d’un système d’information susceptible d’améliorer significativement leur fonctionnement par le biais de la standardisation. Pour autant, les dirigeants d’Abbott ont précisé que la société continuerait également à servir et à développer le portefeuille clients de Starlims hors du secteur de la santé.
VIE DES SOCIETES Renforcer les liens du sang
L’entreprise américaine Haemonetics Corporation spécialisée dans le domaine des solutions de traitement et de gestion du sang et des produits sanguins a signé l’accord définitif d’acquisition de son partenaire européen Global Med Technologies, Inc., maison mère de l’entreprise française Inlog. Le montant de cette opération s’élève à 60 millions de dollars (près de 44 millions d’euros). Les deux sociétés collaboraient déjà depuis 2008 via leurs filiales respectives, Wyndgate et Inlog, dont les activités complémentaires permettent de couvrir l’ensemble des opérations nécessaires à la chaîne d’approvisionnement en sang, depuis le recrutement des donneurs, jusqu’à la redistribution. Haemonetics fournit des solutions pour la collecte, les techniques de séparation et l’utilisation du sang. Pour sa part, Global Med Technologies commercialise une gamme de logiciels de gestion de l’information pour les centres de recueil, les laboratoires et les centres de transfusion. Selon les deux partenaires, cette acquisition vise à offrir à leurs clients des solutions intégrales de gestion du sang, pour améliorer ce pan incontournable des soins cliniques, tout en réduisant les coûts et en respectant les conformités réglementaires et les exigences de qualité le caractérisant.
VIE DES SOCIETES Du soft au middle, Siemens fait le relais
Entre systèmes de gestion de laboratoire et solutions middleware, Siemens Healthcare Diagnostics a fait son choix. En effet, après l’arrêt de la distribution des solutions de Technidata Medical Software (voir Spectra Biologie 117, p. 8), le groupe a annoncé la signature d’un accord de distribution sur le marché français des produits middleware de la société française Clarisys. Siemens Healthcare Diagnostics assurera la promotion, la vente, l’installation et le support de OneLinkTM 2.0, une solution permettant de gérer, tracer et optimiser l’ensemble du workflow pré et post-analytique grâce à des outils totalement intégrés au processus analytique. Ce middleware permet de connecter divers automates, indépendamment du constructeur, sur un ou plusieurs systèmes de gestion de laboratoire afin de mutualiser l’ensemble de la gestion technique sur un même outil. OneLink est adapté aux structures multisites, chaque site possédant une licence différente. Utilisant les protocoles de communication standards (HPRIM ou ASTM), OneLinkTM 2.0 a également été conçu pour potentialiser la puissance des automates Siemens.
VIE DES SOCIETES bioMérieux persiste et Chine
Implanté en Chine depuis 1992 grâce à sa filiale shanghaienne, bioMérieux entend bien prendre part à l’expansion du marché chinois du diagnostic in vitro. Pour ce faire le groupe français a annoncé l’acquisition d’un fabricant chinois de tests rapides, Meikang Biotech et de son site de production basé à Shanghai. BioMérieux mise sur cette opération pour se renforcer sur le marché du diagnostic auprès du patient (point-of-care) et des tests rapides, dans les pays émergents et développés. Stratégiquement situé entre le centre de Shanghai et son aéroport international, Meikang Biotech dispose d’un site de deux hectares regroupant des laboratoires de R&D, des bureaux pour les activités commerciales et 9 000 m² de locaux de production certifiés GMP et ISO où 30 millions de tests sont fabriqués chaque année. La société chinoise possède une large gamme de tests rapides ciblant des maladies infectieuses et cardiovasculaires ainsi que des cancers. Bon nombre de ces produits sont marqués CE, et certains ont reçu l’agrément 510k de la FDA américaine. Mais il ne s’agit là que d’une étape pour le groupe français. En effet, bioMérieux prévoit d’installer d’ici mi-2010 sur le site de Shanghai son siège Grande Chine, son bureau de représentation en Asie-Pacifique, certaines fonctions corporate ainsi qu’un centre de formation pour les clients de la zone Asie-Pacifique.
VIE DES SOCIETES Et en Europe…
Toujours dans le domaine du diagnostic auprès du patient, le groupe de Marcy l’Etoile a également annoncé la signature d’un accord de collaboration avec le néerlandais Philips. Les deux partenaires ont pour objectifs de développer et de commercialiser de nouvelles solutions de diagnostic portables entièrement automatisées, destinées à être utilisées en milieu hospitalier. Ce partenariat mise sur l’alliance des compétences de Philips dans le secteur médical (monitorage des patients, informatique médicale et systèmes d’aide à la décision clinique) et de l’expertise de bioMérieux dans le domaine des biomarqueurs et du développement de tests. La première commercialisation des produits est prévue pour 2013.
VIE DES SOCIETES Quidel intègre Diagnostic Hybrids
Quidel, une société américaine spécialisée dans le développement et la commercialisation de tests rapides type point-of-care a annoncé l’acquisition de son compatriote Diagnostic Hybrids pour un montant de 130 millions de dollars environ, soit plus de 92 millions d’euros. Basée à Athens dans l’Ohio, Diagnostic Hybrids produit et commercialise auprès des hôpitaux et des laboratoires de référence des tests de diagnostic in vitro par fluorescence directe ciblant diverses pathologies, infections (virus respiratoires, Herpès, Chlamydia…) et maladies thyroïdiennes. Quidel entend profiter du portefeuille de produits de Diagnostic Hybrids pour diversifier son offre dans le domaine des maladies autoimmunes et des infections non saisonnières. Quidel commercialise en direct sa gamme de produits QuickVue® aux Etats-Unis au Japon et en Scandinavie, et par l’intermédiaire de bioMérieux dans le reste du monde. La société prévoit de gérer Diagnostic Hybrids comme une filiale séparée et maintiendra à sa tête son actuel président, le Dr Scholl, qui est également nommé vice-président senior de Quidel.
VIE DES SOCIETES Danaher mise sur les technologies médicales
Le conglomérat industriel Danaher poursuit le développement de sa branche d’activité dédiée au secteur des technologies médicales. Après le rachat d’AB Sciex au cours du dernier trimestre 2009 (voir Spectra Biologie 176, p. 14), le groupe américain a annoncé l’acquisition de la société britannique Genetix Group plc le 8 janvier pour un montant total de plus de 73 millions d’euros. Genetix détient des solutions pour l’imagerie et l’analyse d’image intelligente, utilisées pour le développement de produits pharmaceutiques et biothérapeutiques dans les domaines de la recherche et du diagnostic clinique. L’acquisition permettra de combiner ces logiciels d’imagerie avec les scanners numériques Leica de Danaher, pour offrir une technologie de pointe au visionnage d’image numérique de cellules. Genetix gagne ainsi de nouveaux capitaux et de nouveaux marchés. Lawrence Culp, CEO de Danaher, avait déclaré dès novembre dernier vouloir concentrer les investissements de l’entreprise sur la technologie médicale, les tests et instruments de mesure, l’équipement dentaire et les technologies d’identification de produit.
VIE DES SOCIETES Nouveaux marqueurs précoces du diabète
La société américaine Intrinsic Bioprobes (Tempe, Arizona) spécialisée dans le domaine de la découverte de nouveaux biomarqueurs a annoncé avoir cédé à Ortho-Clinical Diagnostics des licences exclusives concernant deux nouveaux marqueurs du diabète. Ces deux biomarqueurs sont des formes modifiées de protéines circulantes et se trouvent associés au pré-diabète ainsi qu’au diabète de type 2. La découverte de ces marqueurs est le fruit d’une collaboration menée avec des chercheurs de l’Université de Yale, ces travaux ayant bénéficié d’un soutien financier de deux millions de dollars (1,44 millions d’euros environ) accordé par les National Institutes of Health.
VIE DES SOCIETES Inverness Medical Innovations enrichit son portefeuille
Poursuivant le développement d’une offre intégrée dans le domaine du diagnostic et des solutions de management de la santé, le groupe Inverness Medical Innovations a encore enrichi son portefeuille produits grâce à plusieurs opérations réalisées en janvier et février derniers. Début janvier, le groupe de Waltham a annoncé avoir conclu un accord de distribution exclusif avec la société canadienne Epocal (Ottawa). Cet accord permet à Inverness de compléter son offre de test d’urgence grâce à l’automate Epoc®, un système de mesure des gaz du sang intégrant de nouvelles technologies de communication et de gestion des analyses au chevet du patient. Ce système est basé sur l’utilisation d’un consommable à usage unique. Approuvé par la FDA, il devrait bénéficier du marquage CE dans le courant de l’année 2010. Par ailleurs les deux partenaires travailleront de concert au développement de nouveaux tests afin d’enrichir cette plateforme. Inverness a aussi étendu sa couverture géographique et s’est offert une porte d’entrée vers l’Asie en devenant actionnaire majoritaire de Standard Diagnostics, une société engagée dans le développement de tests de diagnostic rapide en Corée du Sud. Enfin, le 3 février le groupe de Waltham a annoncé une nouvelle acquisition, celle de Kroll Laboratory Specialists, une division du groupe Kroll spécialisée dans la fourniture de produits et de services dédiés à l’analyse des substances addictives dans le domaine médico-légal aux Etats-Unis.
VIE DES SOCIETES Roche donne du souffle à Kinaxo
La technologie d’analyse protéomique PhosphoScoutTM de la société de biotechnologie allemande Kinaxo intéresse beaucoup le groupe Roche Diagnotics. La preuve ? Roche Diagnostics vient d’entamer un second accord de collaboration avec Kinaxo afin d’appliquer PhosphoScoutTM au développement de thérapies ciblées. Le succès de la plate-forme de spectrométrie de masse quantitative de Kinaxo résulte du besoin croissant pour les sociétés du secteur pharmaceutique de mieux connaître les sites de phosphorylation des protéines cellulaires, des sites fréquemment impliqués dans les mécanismes de régulation de la cellule. PhosphoScoutTM peut cibler jusqu’à 15 000 sites de phosphorylation en un test, facilitant ainsi une analyse globale du phosphoprotéome dans les échantillons des patients, les modèles animaux et les cultures cellulaires. Elle ne nécessite pas d’anticorps pour la détection ce qui permet des analyses complètes du phosphoprotéome à travers des voies entières de signalisation, contrairement aux immunoanalyses pour lesquelles peu d’anticorps spécifiques aux sites de phosphorylation sont disponibles. La première collaboration entre les deux partenaires, débutée en octobre 2009, portait sur l’utilisation de la plate-forme PhosphoScout pour identifier des biomarqueurs associés à de nouvelles approches thérapeutiques basées sur l’utilisation d’anticorps.
VIE DES SOCIETES Cancer : deux nouveaux dépistages précoces disponibles
Doublé gagnant pour Abbott qui vient d’obtenir les approbations européennes nécessaires à la commercialisation en Europe de deux nouveaux tests de dépistage de cancers. Abbott RealTime mS9 est le premier test moléculaire automatisé détectant dans des échantillons sanguins un marqueur du cancer colorectal : la forme méthylée du gène Septine 9. Servant à répondre de l’utilité d’examens plus approfondis, ce nouveau test a pour ambition de réduire la mortalité par cancer colorectal grâce à de meilleurs dépistages. En effet, sa détection précoce offre une issue positive dans 90 % des cas. Concernant le marché français, Abbott mise sur une autorisation de ce test dans le courant de l’année 2010. Il s’agit également du premier test de dépistage d’un cancer disponible sur le système diagnostic par PCR m2000 d’Abbott. Le second test, ARCHITECT HE4, est basé sur l’utilisation de la protéine HE4 et a été développé avec la société américaine Fujirebio (Malvern, Pennsylvanie). Des études ont montré que ce nouveau biomarqueur utilisé conjointement avec le CA125, permet d’estimer le risque de cancer de l’ovaire en préménopause et chez les femmes ménopausées présentant une masse pelvienne. Ce test vient également d’être soumis à la Food and Drug Administration.
VIE DES SOCIETES Cancer du sein : en savoir plus pour mieux traiter
bioTheranostics, la filiale du groupe bioMérieux spécialisée dans le développement de tests moléculaires destinés à aider les praticiens dans le choix de traitements personnalisés contre le cancer, vient d’annoncer un accord commercial avec la société espagnole Ferrer inCode (Barcelone). Concrètement l’entreprise catalane assurera la commercialisation du test THEROS CancerTYPE ID® dans la péninsule ibérique, en Grèce et au Venezuela. Ce test a été conçu afin d’améliorer la classification des cancers, notamment dans le cas de patients souffrant d’un cancer métastatique dont l’origine est incertaine ou inconnue. Selon les termes de l’accord, le test sera commercialisé par la société espagnole et réalisé par bioTheranostics dans son laboratoire californien certifié CLIA et accrédité par le collège américain des pathologistes.
VIE DES SOCIETES Qiagen, partenariat asiatique et acquisition européenne
La filiale de la zone Asie-Pacifique de Qiagen a validé un accord de partenariat avec la société chinoise WuXi AppTec (Shanghai). Les deux entreprises souhaitent s’associer pour fournir à leur clients respectifs une solution intégrée dédiée au développement et à la validation de biomarqueurs moléculaires. Qiagen fournira de l’instrumentation, des consommables et une formation appropriée au personnel de la société chinoise. Cette dernière mettra à disposition ses laboratoires et ses équipes afin de réaliser les services proposés. Les deux partenaires travailleront également de concert au développement de nouveaux panels de biomarqueurs ainsi qu’à la mise au point de tests diagnostics destinés au domaine de la médecine personnalisée. Cette opération s’inscrit pour Qiagen dans la continuité de ses récentes acquisitions, DxS et SABiosciences, spécialisées dans le domaine des biomarqueurs et de la médecine personnalisée. Poursuivant son développement dans le domaine de l’instrumentation, Qiagen a également fait l’acquisition de la société allemande ESE, pour un montant de 14 millions d’euros. Spécialisée dans le domaine des systèmes de mesure optique, ESE dispose d’une technologie de détection de fluorescence a priori très prometteuse. Cette technologie miniaturisée serait particulièrement adaptée au développement de systèmes de diagnostic moléculaire de type point-of-care mais également exploitable dans des appareils de paillasse. Autres atouts, elle permet la réalisation de tests moléculaires extrêmement rapides, estimés entre 5 et 15 minutes et se révèle peu onéreuse à industrialiser. Qiagen entend valoriser cette technologie dans des systèmes de terrains destinés aux secteur de la santé humaine et animale, de l’industrie agroalimentaire et de l’environnement.
PROFESSION Réforme de la biologie médicale
Après 33 ans d’un cadre juridique inchangé, un rapport de l’IGAS en 2006, le rapport du conseiller Michel Ballereau en 2008, des débats animés entre les différentes composantes de la profession et le législateur, la réforme de la biologie médicale a enfin vu le jour. L’ordonnance publiée au JO du 15 janvier 2010 a pour but de moderniser la profession pour s’adapter aux innovations médicales et scientifiques. Elle pose comme fondement la médicalisation de la discipline : l’examen de biologie se pratique en concertation avec le clinicien, et le biologiste en devient garant. Ce point appuie les autres articles qui visent à harmoniser le fonctionnement entre LBM publics et privés en leur reconnaissant un niveau équivalent de fiabilité et en facilitant leur coopération. La réforme doit également garantir une offre continue sur un même territoire et instaure pour cela des règles précises en matière de regroupements, d’achat ou de fusion de laboratoires, en fonction de leur territoire et de la quantité d’examens réalisés dans la région. Du point de vue de l’acte, l’ordonnance incite à l’utilisation des référentiels, notamment ceux publiés par la HAS. L’accréditation devient obligatoire à partir du 1er novembre 2016, l’entrée des LBM dans cette démarche devant être prouvée dès le 1er novembre 2013.
PROFESSION HbA1c, les fruits de la standardisation
L’association américaine du diabète (American Diabetes Association) a publié ses recommandations 2010 de pratique clinique. Le volet diagnostic du document marque cette année une évolution majeure avec pour la première fois la prise en compte de l’HbA1c comme critère permettant de poser le diagnostic de diabète. Plus précisément le document de l’ADA propose le diagnostic de diabète pour les niveaux d’HbA1c supérieurs ou égaux à 6,5 %, dès lors que la mesure a été effectuée au moyen d’une méthode certifiée par le NGSP (National Glycohemoglobin Standardization Program) et standardisée suivant la référence du DCCT (Diabetes Control and Complications Trial). L’association précise que les tests de types point-of-care ne sont pas encore assez précis pour être utilisés. Les avantages et les inconvénients associés à la mesure de l’HbA1c comparativement à la réalisation d’un test de glycémie à jeun sont également évoqués. Par ailleurs, l’ADA suggère la réalisation d’un test HbA1c au moins deux fois par an pour les patients qui satisfont à leurs objectifs de traitement et 1 par trimestre pour ceux dont le traitement a changé ou dont les objectifs glycémiques ne sont pas respectés.
PROFESSION Reconnaissance des réseaux régionaux de cancérologie
La procédure de reconnaissance des réseaux régionaux de cancérologie (RRC) a été lancée par l’INCa et mise en ligne le 19 janvier. Désormais, tout établissement public ou privé voulant traiter des patients atteints de cancer devra appartenir à l’un de ces réseaux. Les RRC découlent de la mesure 29 du plan de mobilisation nationale contre le cancer 2003–2007, et ont en charge la coordination des différents intervenants de la prise en charge des patients. La procédure de reconnaissance, validée par la DHOS, la CNAMTS et l’INCa, définit les cinq critères obligatoires pour être reconnus par le Président de l’INCa : la diffusion des référentiels de pratiques cliniques ; la communication et le partage entre professionnels de santé ; l’information du public et des professionnels ; l’aide à la formation continue et enfin l’observation et l’évaluation des pratiques. Ayant pour but l’amélioration continue des pratiques en cancérologie, il ne s’agit pas d’un réseau de prise en charge ou d’inclusion directe du patient, mais d’une structure permettant d’assurer aux patients une équité d’accès aux soins et des prises en charge de qualité. Leur reconnaissance s’appuiera sur une convention tripartite (INCa, Missions Régionales de Santé et RRC) de 3 ans renouvelables, et fera l’objet d’un suivi annuel qui s’inscrira en complément du tableau de bord régional qui donne lieu depuis trois ans à la publication d’un rapport de synthèse national par l’INCa.
PROFESSION On ne change pas une équipe qui gagne
bioMérieux et le CEA ont annoncé à la fin de l’année dernière un partenariat stratégique à long terme pour renforcer leur collaboration de recherche sur le développement de technologies innovantes de diagnostic des maladies infectieuses. bioMérieux souhaite ainsi rester à l’avant-garde de l’innovation en microbiologie et développer de nouveaux produits de diagnostic rapide et personnalisé. L’expertise du groupe industriel en matière de biosciences, microbiologie, développement de systèmes, production, affaires réglementaires et services clients sera mise au service des solutions émergeant de ces travaux. Cette collaboration profitera d’un accès aux technologies avancées du CEA pour l’imagerie, le traitement et l’analyse des données, les nanotechnologies et les méthodes de détection ultrasensible de molécules. Pendant quatre ans, une centaine de scientifiques de bioMérieux en France et du CEA de Grenoble et de Saclay œuvreront à des projets communs, essentiellement sur les méthodes de détection et d’identification bactérienne rapides grâce aux nouvelles techniques de spectroscopie ou d’imagerie. Les deux partenaires collaborent déjà depuis une dizaine d’années, au sein d’unités de recherche mixtes à Saclay et à Grenoble (France), où bioMérieux a d’ailleurs créé le Centre Christophe Mérieux, dédié à la biologie moléculaire et aux microsystèmes, à proximité du CEA.
SCIENCES Une puce pour détecter les virus émergents
Détecter en 24 heures un agent infectieux connu ou l’un de ses variants émergents dans des échantillons complexes… La tâche n’a rien d’aisée mais pourrait se trouver grandement facilitée grâce aux travaux d’équipes du CNRS (unité d’Epidémiologie et physiopathologie des virus oncogènes) et de l’Institut Pasteur (Cellule d’intervention biologique d’urgence). Ces scientifiques ont en effet mis au point une puce à ADN permettant la détection et l’identification d’un virus ou d’une bactérie parmi un très large spectre d’agents infectieux en situation clinique complexes. Au cœur du terrain expérimental qu’offrait l’épidémie de grippe A (H1N1), ce dispositif a pu révéler la présence du variant viral dans les échantillons des malades mais également déterminer les espaces géographiques et la période de circulation de plusieurs virus H1N1 saisonniers et d’origine porcine testés, ainsi que l’origine, aviaire ou porcine, des différents segments du virus variant. Le système couvre une large diversité génétique virale et possède de grandes capacités de discrimination, même en présence d’un mélange de virus. Cet outil n’a pas été conçu à des fins de diagnostic individuel. Toutefois, son utilisation dans des contextes épidémiques pourrait assister les autorités de santé dans des prises de décisions, notamment concernant le traitement des patients. De futurs développement viseront à étendre encore ses capacités d’identification virale.
SCIENCES Nouveau marqueur pronostic de l’agressivité du cancer de la prostate
Disposer d’un marqueur capable de prédire de façon précise l’agressivité du cancer de la prostate constituerait une avancée notable susceptible de réduire la mortalité et la morbidité associées à cette maladie. En cherchant à déterminer le rôle joué par le gène DAP2IP dans la transition épithélio-mésenchymateuse (TEM), des chercheurs chinois et américains ont peut-être identifié un marqueur pronostic d’intérêt. Ces travaux sont partis de l’observation qu’un polymorphisme de nucléotide simple du gène DAB2IP était associé à un risque de forme agressive du cancer de la prostate. Les scientifiques ont démontré que la perte d’expression du gène DAB2IP initie la TEM alors que sa restauration dans des cellules métastasiques inverse le phénomène. Par ailleurs, chez des souris modifiées porteuses d’une tumeur prostatique humaine, l’absence d’expression de DAB2IP entraîne le développement de multiples nodules lymphomateux et des métastases distantes. L’ensemble de ces investigations a permis de démontrer que le produit du gène DAB2IP constituait une protéine jouant un rôle régulateur clé dans la prévention de l’EMT en modulant l’activité de la béta-caténine. Au final, DAB2IP pourrait donc s’imposer comme un marqueur potentiel du risque de métastase du cancer de la prostate mais également représenter la base d’une nouvelle stratégie thérapeutique.
SCIENCES Vers un traitement pour le « Faux Sida »
Important déficit immunitaire des lymphocytes T CD4, maladies opportunistes… La lymphocytopénie T CD4 idiopathique n’est pas sans rappeler le Sida et peut être mortelle si elle atteint le système nerveux central. Différence notable : aucun agent infectieux étiologique n’a pu être identifié chez les malades, rendant problématique la recherche de traitement et de prévention. Un espoir émerge cependant des travaux de chercheurs et de cliniciens de l’Institut Pasteur, de l’AP-HP, de l’Inserm, du CNRS et de l’université Paris-Descartes. Ces équipes ont en effet mis en évidence un mécanisme physiopathologique commun à six cas français, et ont montré l’efficacité d’un traitement. L’étude moléculaire a révélé une anomalie de l’expression membranaire d’un récepteur majeur du système immunitaire, le CXCR4, co-récepteur d’entrée du VIH dans les CD4. Ce récepteur s’accumule dans le lymphocyte au lieu de s’insérer en surface, perturbant la cellule et ouvrant la voie aux maladies opportunistes. Fort de ce nouvel éclairage, les chercheurs ont testé un traitement par Interleukin-2, molécule messagère du système immunitaire, et ont observé in vitro et chez les patients, une restauration de l’expression de CXCR4 en surface, ainsi que la survie des CD4. Les tests cliniques de ce traitement par immunothérapie sont déjà programmés par l’AP-HP et l’Institut Pasteur sur une cohorte nationale de patients.
SCIENCES Le « French Paradox » enfin dévoilé
Les bénéfices pour le système cardiovasculaire d’une consommation modérée de vin rouge ont fait l’objet de nombreuses études épidémiologiques. On savait depuis plusieurs années que les polyphénols du vin étaient responsables d’un effet vasodilatateur via la production de monoxyde d’azote (NO) par les cellules endothéliales. Toutefois, le mécanisme moléculaire précis de ce que les Anglo-saxons dénomment avec envie le « French Paradox » restait à démontrer. Des travaux d’une équipe Inserm d’Angers contribuent à lever le voile sur la question. Se basant sur une intuition, celle de l’implication du récepteur aux oestrogènes (ER), les chercheurs angevins ont émis l’hypothèse qu’un composé activateur d’un sous type a du récepteur aux oestrogènes (ERa) pourrait suffire à allumer la voie NO dans les cellules endothéliales et induire ainsi la réduction admise du risque de maladies cardiovasculaires. De fait, les polyphénols du vin rouge, en particulier la delphinidine, conduisent au relâchement vasculaire dépendant de l’endothélium dans les artères issues de souris sauvages. En revanche, cette dilatation disparaît en cas d’absence de ces récepteurs, si leur expression n’existe plus ou encore lorsqu’ils sont inhibés pharmacologiquement par un antagoniste. En complément, la modélisation moléculaire ainsi que des études de liaisons spécifiques ont confirmé l’interaction directe de la delphinide sur le site activateur du récepteur ERa. Ainsi, l’ensemble de ces résultats vient fournir une base scientifique aux hypothèses issues des études épidémiologiques sur les effets protecteurs vasculaires de la consommation modérée de vin et d’autres végétaux. In vino salus !
 |
Également dans Spectra Biologie n° 178 |
- un point sur Accréditation, informatique et robotique : les clés d’une évolution
- cas bioclinique Intoxication par les pesticides organophosphorés : comment l’analyse toxicologique peut aider le clinicien à améliorer la prise en charge d’un patient intoxiqué ?
- laboratoire pratique Des interférences sur le dosage de TSH pratiqué sur certains automates d’immunoanalyse à l’origine de diagnostics erronés d’hypothyroïdie fruste
- Technologie appliquee Accréditation en hémato-cytologie
Pour recevoir notre revue dans son intégralité, rendez-vous sur notre site
pour découvrir nos offres d’abonnement au format presse ou au format électronique.
pour découvrir nos offres d’abonnement au format presse ou au format électronique.
 |
Manifestations |
>> 3es Journées Nationales de Biologie Praticienne de l’AMBM
TANGER (Maroc) – 02–03 avril
>> 1er Congrès International Francophone de la FIFBCML
et XXIVes Journées Nationales de Biologie Clinique
et XXIVes Journées Nationales de Biologie Clinique
HAMMAMET (Tunisie) – 28 avril-1er mai
>> 3e Réunion annuelle de la COMETH
PALAVAS-LES-FLOTS – 06–07 mai
>> 1ère journée des biomarqueurs de la Pitié-Salpêtrière
PARIS – 07 mai
• Tél. : 01 42 17 72 42
>> 30e Journée Normande de Biologie Clinique
HEROUVILLE-SAINT-CLAIR – 20 mai
• Tél. : 02 31 69 01 76 Contact mail
>> 18es Journées Toulousaines de Biologie Médicale
TOULOUSE – 27–28 mai
• Tél. : 05 34 56 90 35 Contact mail
>> 8e Congrès national de la Société Française de Microbiologie (SFM)
MARSEILLE – 02–04 juin
La Newsletter Spectra Biologie est une publication des éditions PCI
176, rue du Temple – 75003 Paris
Tél. : 01 44 59 38 38 – Fax : 01 44 59 38 39
www.editions-pci.com – pci@editions-pci.fr
176, rue du Temple – 75003 Paris
Tél. : 01 44 59 38 38 – Fax : 01 44 59 38 39
www.editions-pci.com – pci@editions-pci.fr
